Использование препаратов Хелль у кошек с хроническим заболеванием почек: многоцентровое, проспективное, наблюдательное исследование

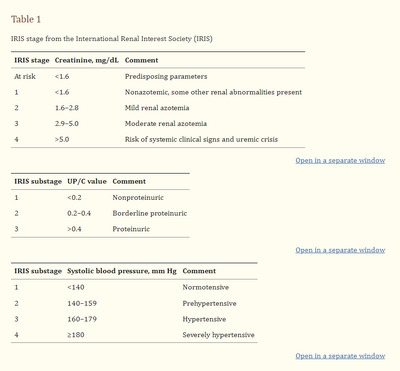
Перевод статьи Brandenburg U, Braun G, Klein P, Reinhart E. The Multicomponent, Multitarget Therapy SUC in Cats with Chronic Kidney Disease: A Multicenter, Prospective, Observational, Nonrandomized Cohort Study. Complement Med Res. 2020;27(3):163-173. doi: 10.1159/000506698. Epub 2020 Mar 26. PMID: 32213769; PMCID: PMC7384345. Аннотация Предыстория Мы сравнили многокомпонентный препарат SUC (Solidago compositum ad us. vet., Ubichinon compositum и Coenzyme compositum, Heel GmbH, Баден-Баден, Германия) с известным ингибитором ангиотензин-превращающего фермента беназеприлом в проспективном, обсервационном, нерандомизированном, когортном исследовании кошек с хронической болезнью почек (ХБП). Целью исследования было оценить переносимость и эффективность SUC у кошек с ХБП. Материалы и методы: Сто тридцать шесть кошек были обследованы на наличие Х, и 70 кошек были допущены к участию в исследовании. Тридцать три кошки были направлены на лечение SUC, а 35 кошек получали беназеприл. Всем кошкам был поставлен диагноз ХПН. Период наблюдения составил 168 дней. Ответ оценивался как улучшение или стабильность уровня креатинина в сыворотке крови по сравнению с исходным уровнем до конца исследования. Кроме того, оценивался клинический суммарный балл, как показатель качества жизни. Результаты Уровень креатинина в сыворотке крови оставался близким к исходному в обеих группах исследования с небольшим улучшением в группе SUC. Сводный клинический балл значительно улучшился в группе SUC на 3, 7, 28, 56 и 112-й дни, но не на 168-й день. Выводы С учетом ограничений, наложенных на исследование, полученные результаты позволяют говорить о целесообразности применения SUC в качестве нового интересного метода лечения ХПН у кошек. Результаты показывают, что SUC может быть более эффективным, если давать его не менее двух раз в неделю. Ключевые слова: кошки, Solidago compositum ad us. vet., Ubichinon compositum, Coenzyme compositum Справочная информация Хроническая болезнь почек (ХБП) у кошек определяется как потеря функции почек [1]. В последние десятилетия ХБП диагностируется все чаще [2, 3], и были выявлены факторы риска, связанные с развитием ХБП [4]. Особенно у кошек, почечные заболевания являются причиной смертности номер один у животных в возрасте до 5 лет [5, 6, 7, 8]. Симптомы ХБП зависят от степени тяжести заболевания. Общими признаками ЦП являются вялость, снижение аппетита и, как следствие, потеря веса, что предполагает снижение качества жизни [9]. Кроме того, часто наблюдаются полиурия/полидипсия, повышенная концентрация креатинина, обезвоживание, протеинурия и снижение удельного веса мочи (УГМ) [10]. Диагностическое обследование должно включать полный анализ крови, биохимический анализ сыворотки, анализ артериального давления и анализ мочи с определением соотношения белка и креатинина в моче (UP/C) [10, 11]. Международным почечным обществом (IRIS) была разработана система стадирования для кошек с ХБП [12] (табл. 1.1). Наиболее сильными предикторами выживаемости являются сывороточный креатинин и УП/С [13]. ХБП - необратимое и прогрессирующее заболевание [14, 15], и лечение направлено на сохранение функции почек и поддержание хорошего качества жизни [10]. Рекомендации по лечению ХБП у кошек включают корректировку рациона с ограничением белка и фосфатов, а также, при необходимости, контроль калийного баланса и анемии [16, 17, 18, 19, 20]. Кроме того, при наличии протеинурии часто назначается фармакотерапия. При почечной протеинурии ингибиторы ангиотензин-превращающего фермента (ИАПФ) входят в стандарт лечения как у кошек, так и у собак [19, 21, 22, 23, 24]. Комбинированное лечение препаратами Solidago compositum ad us. vet. (Heel GmbH, Баден-Баден, Германия), Ubichinon compositum (Heel GmbH, Баден-Баден, Германия) и Coenzyme compositum (Heel GmbH, Баден-Баден, Германия) с многочисленными ингредиентами был разработан в качестве интегративного лечения кошек с ХБП по принципу многокомпонентного и многоцелевого воздействия. В дальнейшем используется аббревиатура SUC (Solidago ad us. vet., Ubichinon compositum и Coenzyme compositum). У большинства кошек с диагнозом ХБП хронический тубулоинтерстициальный нефрит и почечный фиброз являются обычными гистологическими находками [25, 26, 27]. У людей тубулоинтерстициальный нефрит и почечный фиброз были связаны с клеточным старением в почечной ткани [28, 29]. Сенильные клетки экспрессируют провоспалительные цито- и хемокины, вызывая воспаление, фиброз и потерю функции органов [28]. Предотвращение перехода от нормальных к сенесцентным клеткам связывают с Solidago virgaurea, основным ингредиентом Solidago compositum ad us. vet. [30]. Кроме того, соединения, выделенные из S. virgaurea, обладают антимикробной, анальгетической, противовоспалительной, спазмолитической и легкой мочегонной активностью [31]. Мочегонная активность S. virgaurea была связана с ингибированием АПФ, сравнимым с действием беназеприла [31]. АПФ играет ключевую роль в развитии ЦП, вызывая гломерулярную гипертензию, приводящую к повреждению гломерул и активации провоспалительных и профибротических путей [32]. Таким образом, S. virgaurea может уменьшать воспаление почечной ткани и защищать функцию органа, предотвращая фиброз. Убихинон композитум и коэнзим композитум могут усиливать митохондриальное дыхание, что приводит к снижению окислительного стресса в тканях-мишенях, вызванного нарушением митохондриальной дыхательной системы [33, 34]. Появляется все больше доказательств того, что снижение дыхательной способности митохондрий может быть причиной или следствием хронических заболеваний почек у пациентов [35, 36, 37]. Несмотря на большой опыт применения SUC, имеется лишь небольшое количество исследований, демонстрирующих эффективность и переносимость SUC у кошек [38, 39, 40]. Основной целью данного многоцентрового, проспективного, двуручного, обсервационного нерандомизированного когортного исследования была оценка переносимости. Второй целью было показать эффективность лечения. В этом клиническом исследовании SUC сравнивали с АПФ беназеприлом у кошек с ЦП. Кроме того, качество жизни оценивали владелец и лечащий ветеринар. Материал и методы
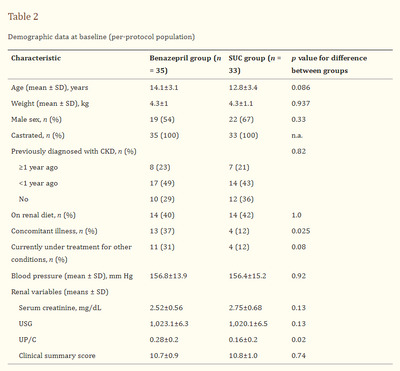
Кошки В период с 2012 по 2016 год в 12 ветеринарных центрах Германии было обследовано 136 кошек, принадлежащих клиентам, в возрасте >12 месяцев, у которых подозревали или знали о наличии ЦП. Семьдесят кошек были включены в исследование (рис. (рис. 1)). Критерии включения В исследование могли быть включены кошки любого пола при наличии информированного согласия владельца. В исследование включались кошки с массой тела 2,0-10 кг. У всех кошек должна была быть диагностирована клинически стабильная ХПН на основании критериев общества IRIS. Определение стадии ХПН по IRIS включает измерение сывороточного креатинина, UP/C (соотношение в моче протеина к креатинину) и артериального давления (табл. (табл. 1).1). Диагноз ХПН устанавливался на основании клинического анамнеза, физикального обследования и результатов лабораторных исследований. Должны были соблюдаться следующие критерии: концентрация креатинина в сыворотке крови ≥2 и ≤5 мг/децилитр и UP/C ≤1,035. К участию в исследовании допускались кошки с суммарным клиническим баллом 10-15. Кошки, получающие почечную диету, допускались к участию в исследовании, если они получали диету в течение не менее 4 недель до включения в исследование; также допускались кошки с сахарным диабетом или гипертиреозом, если сопутствующее заболевание было стабильным в течение не менее 4 недель. Критерии исключения
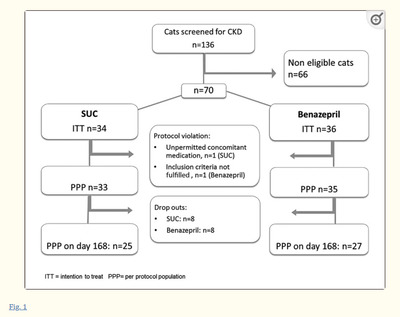
Кошки не допускались к участию в исследовании, если имели креатинин сыворотки крови <2 и >5 мг/дл, суммарный клинический балл ниже 10 или выше 15, бактериальную инфекцию мочевыводящих путей или получали сопутствующее лечение в течение 14 дней до включения в исследование другими ИАПФ, диуретиками, нестероидными противовоспалительными препаратами, кортикоидами, нефротоксичными антибиотиками, противорвотными средствами или стимуляторами аппетита. Кошки, получавшие гомеопатические или растительные препараты за 28 дней до начала исследования и в течение всего периода исследования, исключались. Дизайн исследования Это было многоцентровое, проспективное, обсервационное, двуручное, нерандомизированное, открытое исследование когорты, проведенное в 12 ветеринарных клиниках Германии в период с июля 2012 по июнь 2016 года. Дизайн и проведение исследования соответствовали Руководству по надлежащей клинической практике (GCP) VICH GL9 [41]. Для разработки протокола исследования была привлечена контрактная исследовательская организация (Klifovet AG, Мюнхен, Германия). Подходящие места проведения исследования были выбраны из числа исследователей, имеющих опыт проведения клинических исследований в соответствии с GCP и контроля активной фазы исследования в соответствии с GCP. Участки исследования отвечали за управление данными и представление результатов исследования в компанию Klifovet AG. Места проведения исследований считались подходящими, если они имели опыт применения исследуемого препарата, располагали достаточным количеством пациентов для набора необходимого числа случаев и были оборудованы для сбора клинических данных, например, цистоцентеза. Лечение Кошек лечили либо SUC, либо беназеприлом (таблетки Benefortin® Flavour 2,5 мг; Boehringer Ingelheim Vetmedica GmbH, Ингельхайм, Германия). В каждом центре-участнике все кошки получали либо SUC, либо беназеприл. Чтобы обеспечить правильное лечение либо SUC, либо беназеприлом, центры, знакомые с беназеприлом, лечили всех кошек беназеприлом, а центры, знакомые с SUC, использовали только SUC. Такая схема гарантировала, что ветеринары не смогут сравнить результаты лечения между группами, чтобы уменьшить предвзятость, вызванную неслепым дизайном этого обсервационного исследования. SUC состоит из множества ингредиентов, представленных в дополнительной онлайн-таблице 1. Все компоненты SUC имеют разведения в диапазоне 10/4-10/10. Компоненты смешивались в равных частях, и 3 мл раствора вводились ветеринаром подкожно во время первого визита, после чего владелец давал препарат перорально. Лечение проводилось ежедневно в течение первой недели, каждый второй день на второй неделе, дважды в неделю с 21-го по 55-й день, а затем доза была снижена до одного раза в неделю (рис. (рис. 2).2). Беназеприл давали в дозе 0,5-1,0 мг/кг каждые 24 ч в виде 2,5-мг таблетки в соответствии с инструкцией препарата (кошки с массой тела 2,5-5 кг получали 1 таблетку, а кошки с массой тела >5 кг - 2 таблетки). Стандартизация рациона кошек не проводилась, почечная диета разрешалась, если она была начата за ≥4 недели до зачисления в исследование. Коррекция обезвоживания с помощью инфузии разрешалась в течение периода исследования, но инфузия должна была быть прекращена не менее чем за 48 ч до взятия проб крови и мочи.

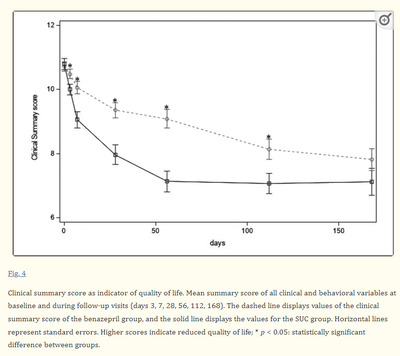
Продолжительность исследования и оценка Кошки находились под наблюдением в течение 168 дней. Клинические обследования проводились на скрининговом визите, на исходном уровне (день 0) и в дни 3, 7, 28, 56, 112 и 168, соответственно, в пределах временного интервала ±1 день до дня 7 и ±3 дня после него. Артериальное давление измерялось неинвазивно во время скринингового визита, а также по возможности на 56-й и 168-й дни. В каждой временной точке проводилось 5 измерений, и рассчитывалось среднее артериальное давление. Мочу собирали во время скрининга и в дни 7, 28, 56, 112 и 168 для определения UP/C и УЗИ. Цистоцентез был предпочтительным методом во всех временных точках. Кроме того, во время скрининга и в дни 7, 28, 56, 112 и 168 проводился полный анализ крови и биохимический анализ крови. Ответ оценивался как снижение или стабильный уровень креатинина сыворотки крови по сравнению с исходным уровнем. Клинические параметры регистрировались во время каждого визита. Клинический суммарный балл Качество жизни оценивалось на каждом визите с помощью клинической суммарной оценки по шкале от 1 до 4 для каждой переменной, согласно Mizutani et al [22]. Сводная клиническая оценка включала 5 переменных, таких как общее поведение, аппетит, рвота, обезвоживание и состояние меха. Сумма всех значений по 5 переменным рассчитывалась и отображалась как суммарный клинический балл, где 5 - наименьшее значение, а 20 - наибольшее. Высокое значение свидетельствует о значительном снижении качества жизни. Общее поведение оценивалось как: 1 = нормальная активность, 2 = легкая астения (легкая слабость), 3 = умеренная астения (умеренная слабость) и 4 = кома. Аппетит оценивался как 1 = хороший аппетит, 2 = слегка сниженный аппетит (>50 % от нормального потребления пищи), 3 = заметно сниженный аппетит (<50 % от нормального потребления пищи) и 4 = полная анорексия. Рвота оценивалась как отсутствие различий в частоте = 1, не ежедневная, но более частая, чем обычно = 2, рвота один раз в день = 3, а рвота более одного раза в день оценивалась как 4. Обезвоживание оценивалось от 1 до 4, где 1 означает отсутствие обезвоживания, а 4 - сильное обезвоживание. Состояние шерсти оценивалось как 1 = нормальное, 2 = несколько спутанностей, редкий уход, 3 = тусклый, спутанный, редкий уход и 4 = тусклый и жирный мех, без ухода. Общая терапевтическая эффективность Общая терапевтическая эффективность оценивалась ветеринаром и владельцем в последний день исследования как 1 = заметное улучшение, 2 = незначительное улучшение, 3 = без изменений и 4 = ухудшение. Данные о безопасности собирались на протяжении всего исследования. Обо всех предполагаемых нежелательных явлениях сообщалось в соответствии со стандартными протоколами фармаконадзора. Соблюдение режима лечения оценивалось путем сбора и подсчета оставшихся таблеток и ампул в конце исследования. Статистические методы
Исследование было спланировано как проспективное, референс-контролируемое, нерандомизированное обсервационное исследование. Использовались стандартные статистические методы с использованием SAS 9.3. Исходные данные сравнивались между группами с помощью теста Вилкоксона для интервальных данных, теста Мантеля-Хаензеля для порядковых данных и точного теста Фишера для бинарных данных. Для сравнения между методами лечения рассчитывали изменения по сравнению с исходным уровнем и различия между группами. Статистические сравнения проводились с помощью ANOVA, теста Мантеля-Хаензеля и точного теста Фишера, в зависимости от ситуации. Для всех сравнений рассчитывали двусторонние 95% доверительные границы. Статистически значимым считалось значение p < 0,05. Вначале исследования UP/C был заметно ниже в группе SUC, сравнение UP/C проводилось с помощью ANOVA с поправкой на баллы склонности - на основе креатинина и UP/C при исходном уровне. Различие SUC по сравнению с беназеприлом оценивалась по переменной ответа - изменению сывороточного креатинина по сравнению с исходным уровнем. Нижняя граница 95 % доверительного интервала для различий между группами лечения через 168 дней была сравнена с 0,6 мг/дл, что считалось в пределах величины изменений, не имеющих клинического значения, а также представляет собой половину разницы в уровне креатинина сыворотки между 2-й и 3-й стадиями IRIS [12]. Одной из целей исследования было показать переносимость SUC по сравнению с терапией беназеприлом, и для этого переменные эффективности были проанализированы в популяции per-protocol. Для оценки достоверности результатов был проведен дополнительный анализ «намерение к лечению». 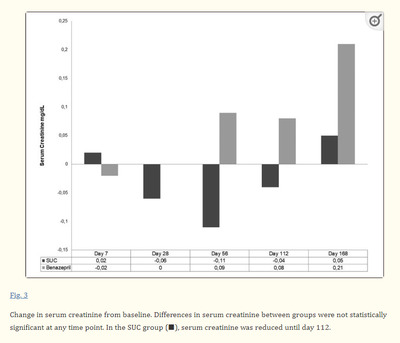
Выводы В целом, данное обсервационное пилотное исследование показало, что эффективность многоцелевой многокомпонентной терапии SUC не уступает по эффективности широко используемому АПФ беназеприла для лечения кошачьей ХПН легкой и средней степени тяжести в течение 168 дней наблюдения. С учетом ограничений, наложенных на исследование, полученные результаты свидетельствуют о целесообразности применения SUC в качестве нового интересного метода лечения ХПН у кошек. Есть также доказательства того, что частота дозирования SUC играет ключевую роль в защите почечной ткани для стабилизации этого смертельного заболевания у кошек. Дальнейшие исследования, включая возможное использование в качестве дополнительной терапии и сравнение с более новыми вариантами лечения, представляются целесообразными. Источник: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7384345/ | |
| Просмотров: 1267 | |
